PBL Fall 5: Njuren 1
Njurens funktion och urinbildning
Fallet
Person dricker mycket och pissar mycket.
Urinet visar sig vara utspätt och ADH nivåerna är låga, precis som plasmaosmolariteten.
Vid törstprov ändras värdena och urinet koncentreras.
Studiemål
Njuren
- • Anatomi
- • Funktion
Hur bildas urin
- • Filtration
- • Reabsorption
- • Sekretion
Permeabilitet
- • Na⁺, Cl⁻, Proteiner
- • Glukos, Urea
- • Ca²⁺, Mg²⁺
Urinvägarna
- • Urinledare
- • Urinblåsa
- • Miktionsreflex
Ord
- • Clearance
- • Sievingskoefficient
Fallet
- • ADH
- • Osmolalitet
Njurens funktioner
Njurens funktioner är många:
- • Utrensning av slagg och främmande produkter ur kroppen
- • Vatten och elektrolytbalans
- • Kroppsvätskor osmolalitet och elektrolytkoncentration
- • Artärtryck: Utsöndrar Renin
- • Syra-bas balans
- • Sekretion, metabolism och utsöndring av hormoner
- • Gluconeogenesis: Glukos från aminosyror
- • Reglerar Erythrocyte produktion: Stimulerar bildandet av röda blodkroppar i benmärgen
- • Reglering av D-vitamin, producerar aktiva formen av D-vitamin, Calcitriol (D3)
Vätska in och ut ur kroppen
En persons intag av vätska varierar kraftigt mellan dagar och personer. Normalt intar man ungefär 2100 ml/dag via vatten och 200 ml/dag via oxidering av kolhydrater.
Från kroppen försvinner sedan passivt "omedvetet" runt 350 ml/dag via huden och diffusion (inte svettning, detta sker även hos folk utan svettkörtlar). En lika stor del, 350 ml/dag går via lungorna som får med sig fukt ut.
Förlust av vätska kan ske snabbt via träning och ökad svettning. Normalt svettas man ungefär 1 dl/dag och vid träning, samt varma klimat, kan det stiga till 1-2 liter/dag.
En liten mängd (1dl/dag) kommer ut genom avföringen (ökar kraftigt vid diarré), medan den stora mängden kommer via njurarna och urinen.
Njurens Anatomisk översikt
Njurarna finns i par och sitter i mitten av buken. Från njurarna går sedan vars en urinledare ner till urinblåsan.
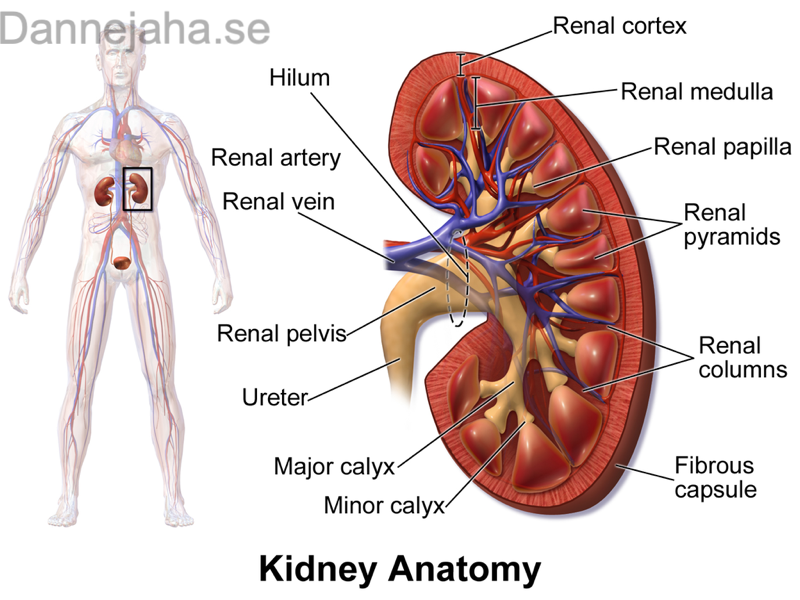
Njurens anatomi - Översikt
Njurfysiologi
Njuren är unik i att den har två kapillärbäddar (Glomerular och Peritubular) i serie och delade av efferenta arterioler. Arteriolerna reglerar hydrostatiska trycket i båda nätverken.
- • Högt hydrostatiskt tryck i Glomerular ger mer filtrering (60 mm Hg)
- • Lågt Hydrostatiskt tryck i Peritubular ger snabbare återabsorption (13 mm Hg)
Nephron
Nephron är den funktionella enhet som sitter mellan Cortex och ner i Medullas Pyramider. Kroppen har ungefär 1,000,000 av dessa och de återbildas inte. Från 40 års ålder börjar de försvinna med ungefär 10% per 10 år.
Nephronens beståndsdelar:
- • Bowman Capsule: Filtrerar blodet
- • Cortical Glomerulus: Omsluten av Bowman Capsule
- • Loop of Henle: Tunn del där nedåtgående och uppåtgående loopen vänder
- • Tubule: Filtrerad vätska blir urin
- • Macula densa: Slutet av tjocka stigande tuben är område med speciella epitelceller
Dess funktion är att:
- • Filtrera (i Glomerulus)
- • Tubulär Reabsorption (Hela Nephronet)
- • Tubulär Sekretion (Hela Nephronet)
Nephronens funktion
Filtrering i Glomerulus
Glomerulusen får in enorma mängder blod som den ska filtrera per dag, men allt kommer inte igenom. Protein och blodkroppar är för stora för att ta sig igenom.
Glomerulär filtration
GFR (Glomerulus Filtration Rate) ligger runt 20% av njurens plasmaflöde och bestäms av:
- • Balansen mellan hydrostatisk och kolloid osmotisk kraft över kapillärerna
- • Kapillärernas filtrations Coefficient (Kf), alltså permeabilitet och area att filtrera genom
Filtrationen här är bättre än i övriga kroppen eftersom det är högre tryck och Kf vilket ger en GFR på ungefär 125 ml/min eller 180 L/dag.
Grundläggande formel
E = F - R + S
E: Mängd i urin
F: Mängd filtrerat
R: Mängd Reabsorberat
S: Mängd Sekrerat
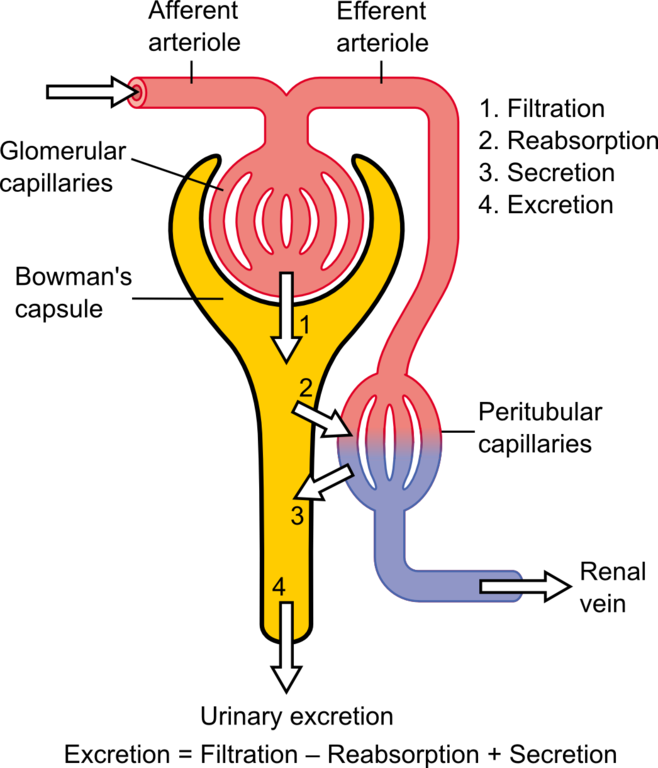
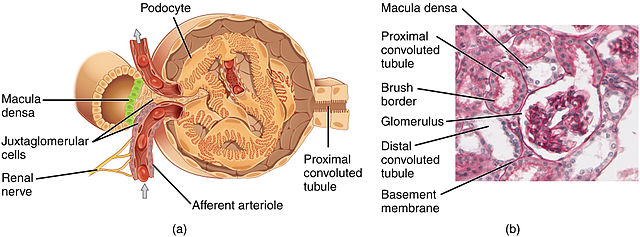
Tubulär Reabsorption och Sekretion
Efter filtrering i Glomerulus kommer en reabsorption och sekretion att ske via tubuli.
Grundformel
Urin excretion = Glomerular Filtration - Tubular Reabsorption + Tubular Secretion
Reabsorption = när blodet tar tillbaka
Sekretion = när blodet avger till tubuli
Aktiv Transport vid reabsorption
Primär aktiv transport
De primära aktiva transporter man känner till i njuren (använder ATP):
- • Natrium/Kalium
- • Vatten
- • Vatten/Kalium
- • Kalcium
Sekundär aktiv transport
När två eller fler substanser samarbetar med ett specifikt membranprotein (carrier-molekyl) och blir tillsammans transporterade över membranet.
Detta är hur aminosyror och glukos hanteras och är så effektivt att i princip allt reabsorberas.
SGLT1 och 2 (Sodium Glucose co-transporters)
Finns i början och slutet av tuben:
- • 90% reabsorberas av SGLT2 som finns i början
- • 10% av SGLT1 som finns i slutet
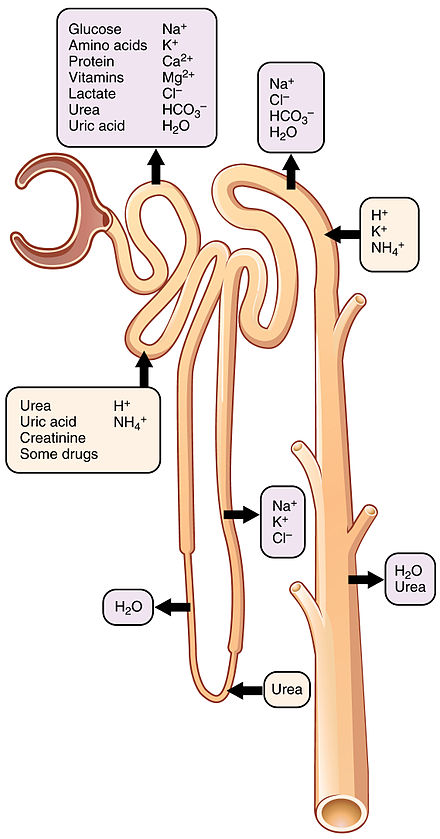
ADH och Urinkoncentration
ADH påverkar olika delar av tubuli. Det är Hypothalamus som säger åt hypofysen att utsöndra ADH. Det är när osmoreceptorer i hypothalamus får signalering om stigande koncentrationer som processen startar och ADH kommer ut i blodet.
ADH:s effekter:
- • Ökar vattenreabsorption genom att öka permeabiliteten i distala tubuli, collecting tubuli och collecting duct epitel
- • ADH binder till V2 receptorer och ökar bildandet av cAMP
- • Aktiverar kinas som startar Aquaporin-2 (AQP-2) som är vid lumen i epitel
- • AQP-2 bildar hål i cellmembranet som släpper igenom vatten
Faktorer som påverkar ADH:
Morfin och Nikotin, illamående ökar ADH nivåerna.
Alkohol minskar ADH nivåerna och förklarar varför man blir mer kissnödig när man dricker alkohol.
Miktionsreflexen
Glatta musklerna i urinblåsan kallas Detrusor Muscle, sträcker sig åt alla håll och kan öka trycket i blåsa med 40-60 mm Hg.

I blåsan finns en triangulärt område kallat Trigone. Från denna triangel bildas sedan urinröret ut och runt här finns mycket elastiska fibrer ihop med den glatta muskulaturen. Detta bildar den interna Sphinkter muskeln.
Reflexen går i 3 steg:
- 1. Progressiv och snabb ökning av tryck
- 2. En period med bibehållet tryck
- 3. Återgående av tryck till basnivå
Nervstyrning:
- • M3 i blåsan: Kontraherar när n. Pelvic (parasympatisk) skickar ut Acetylkolin
- • Nikotinerga: Kontraherar External Sphincter via n. Pudendus
- • β3 och α1 tar emot Noradrenalin från n. Hypogastric (sympatisk)
Miktionsreflex - Video
Clearance
Clearance är ett begrepp inom farmakologi och fysiologi och som är ett mått på den hypotetiska plasmavolym som är helt befriad från en viss substans per tidsenhet.
Clearance formel
Clearance rate = Cs = Us × V / Ps (ml/min)
Us: Urinkoncentrationen av substansen s
V: Urin flödeshastighet
Ps: Plasmakoncentrationen av substans s
Användningsområden:
- • Creatinin för att estimera GFR
- • PAH Clearance för att mäta RPF (Renal Plasma Flow)
- • Filtration Fraction räknas ut med GFR och RPF